Les coliphages sont des virus capables d’infecter les bactéries coliformes comme Escherichia coli, ou plus rarement Shigella spp ou Klebsiella spp. E. coli est la bactérie la plus abondante dans l’intestin humain et animal. De ce fait, les coliphages, virus non pathogènes, sont également les plus abondants dans l’intestin.
Par ailleurs, il a été démontré que les coliphages ne se multiplient que très faiblement dans l’environnement car les conditions leurs sont trop défavorables. Ainsi, les coliphages retrouvés dans l’environnement proviennent principalement de contaminations d’origine fécale et peuvent être utilisés comme indicateurs de la qualité microbiologique de l’eau.
Caractéristiques principales des coliphages
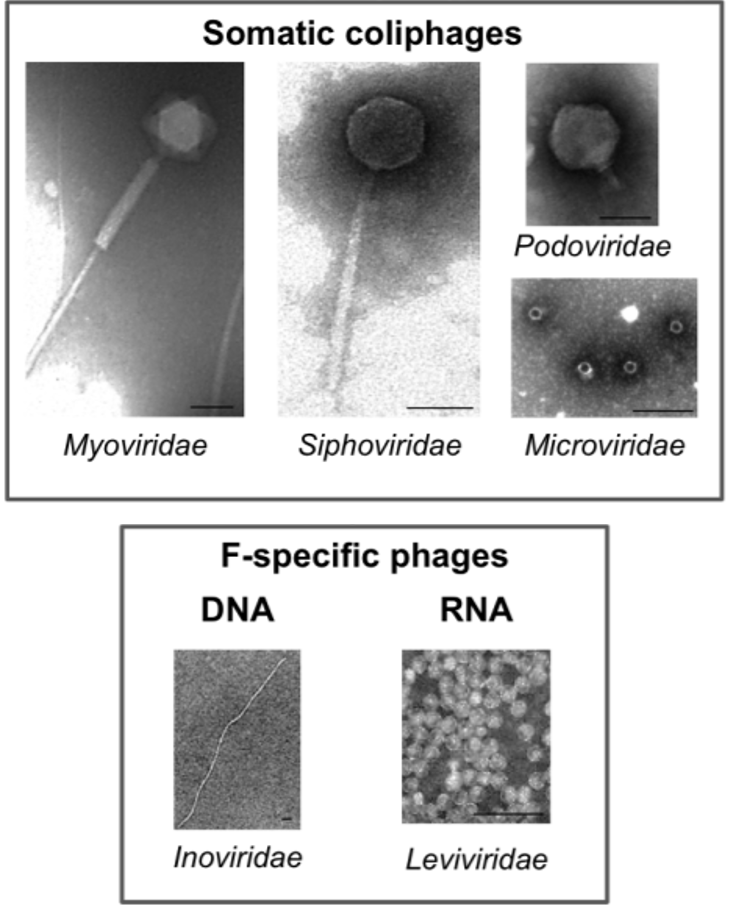
Dans les eaux, on s’intéresse principalement à deux types de coliphages : les coliphages somatiques et les bactériophages ARN F-spécifiques. Ils se distinguent notamment par le récepteur bactérien auquel ils s’attachent pour l’infection.
| Coliphage somatique | Bactériophage ARN F-spécifique | |
| Mode d’infection | Infection par un récepteur de la paroi bactérienne. | Infection par le pilus sexuel de la bactérie. |
| Taille | Très variable (≈ 50-120 nm) | 21-30 nm |
| Génome | ADN simple ou double brin | ARN simple brin |
| Familles les plus connues | Myoviridae, Podoviridae ou encore Microviridae | Leviviridae |
| Modèle le plus utilisé | ϕX174 | MS2 |
Le terme « coliphages totaux », que l’on peut retrouver dans certaines réglementations, regroupe les coliphages somatiques et les bactériophages ARN F-spécifiques.
Quel est le meilleur indicateur de contamination fécale/d’efficacité des traitements ?
Les coliphages somatiques sont-ils un meilleur indicateur de contamination fécale que les bactériophages ARN F-spécifiques ? Ceci est sujet à débat. Les études scientifiques semblent montrer que les coliphages somatiques sont généralement plus abondants dans les eaux que les bactériophages ARN F-spécifiques. Cependant, cela semble être l’inverse dans les eaux souterraines ou les eaux recyclées traitées aux UV. Par ailleurs, d’un point de vue purement méthodologique, la détection des coliphages somatiques est plus simple.
Ce qui est sûr, c’est qu’en comparaison avec les indicateurs bactériens, les coliphages sont moins sensibles aux procédés de désinfection et survivent plus longtemps dans l’environnement. Par ailleurs, les virus migrent plus rapidement et plus loin dans les sols que les bactéries. Ainsi, l’eau peut être contaminée par des virus entériques humains même en l’absence d’indicateurs bactériens traditionnels (bactéries coliformes/E. coli). Le rapport de l’ANSES (n° 2018-SA-0027), publié en 2018, souligne que les bactériophages sont de très bons indicateurs d’efficacité du traitement appliqué à l’encontre de virus.
Que demande la réglementation ?
Depuis quelques années, la réglementation introduit le suivi des coliphages pour contrôler la qualité d’eau aussi bien dans certains états des Etats-Unis ou d’Australie qu’en Europe. Ces nouveaux critères microbiologiques concernent l’eau destinée à la consommation humaine ainsi que les eaux usées traitées. Les réglementations existantes recommandent d’analyser soit la quantité de coliphages somatiques, soit de bactériophages ARN F-spécifiques, soit les deux.
En Europe, le dénombrement des coliphages somatiques est introduit dans la nouvelle Directive Européenne 2020/2184 « Eau potable » au niveau de la ressource. Si le résultat est supérieur à 50 PFU dans 100 ml, l’eau en sortie de filière de traitement doit être contrôle pour démontrer l’efficacité de traitement.
De plus, cette nouvelle directive introduit la mise en place des PGSSE. Ces plans de gestion demandent aux exploitants de mettre en place une stratégie générale de prévention des risques. Ainsi, il est pour eux indispensable de mettre en place de nouveaux indicateurs, comme les coliphages somatiques. Cette révision a été publiée le 23 décembre 2020.
On retrouve également le dénombrement des coliphages en Europe dans la réglementation européenne concernant la réutilisation des eaux usées traitées parue en juin 2020. Cette fois-ci, il est recommandé d’analyser les coliphages totaux en entrée et sortie de STEP. Un abattement de 6 LOG est par exemple demandé suivant la qualité d’eau destinée à l’irrigation agricole.
Comment les détecter ?
Afin de répondre à ces nouvelles exigences réglementaires, les laboratoires doivent mettre en place les méthodes d’analyses adaptées. D’après le rapport de l’ANSES, en 2018 en France, seul un laboratoire était accrédité pour l’analyse des phages, et uniquement pour les bactériophages ARN F-spécifiques.
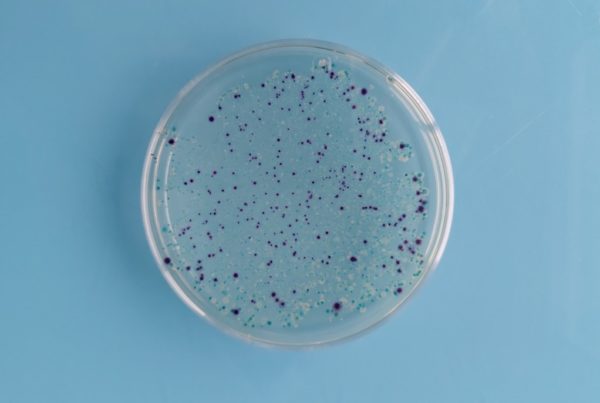
Les normes EN ISO 10705-1 et 10705-2 décrivent la détection par comptage des plages de lyse sur gélose en double couche pour les bactériophages ARN F-spécifiques et les coliphages somatiques respectivement.
Cependant, elles proposent uniquement de déposer 5 ml d’eau sur 20 géloses afin d’analyser les 100 ml d’échantillon. Cette méthode est longue, fastidieuse, couteuse en matériel et donc non adaptée à une analyse en routine.

Toutefois, la partie -3 de cette même norme conseille plusieurs solutions. D’après les études menées sur le sujet, la concentration sur membrane filtrante semble être la plus simple et la moins couteuse à mettre en place. Elle est particulièrement adaptée pour observer les abattement de 4 à 6 LOG demandés, pour l’analyse des eaux présentant une faible turbidité comme l’EDCH ou dans le cadre de la réutilisation des eaux usées traitées.
C’est pour cela que nous proposons le kit de concentration VIRAPREP® déjà utilisé par plusieurs laboratoires d’analyses.